兵庫医科大学化学2013年第2問
次の文章を読み、設問(1)~(6)に答えよ。ただし、気体はすべて理想気体としてふるまい、液体の体積とピストンの重さは無視できるものとする。また、大気圧は$1.0\times10^5$Pa、原子量は$\text{H}=1.0$、$\text{C}=12$、$\text{O}=16$とする。
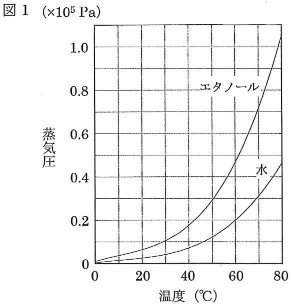

密閉した容器に適量の液体を入れると、最初は蒸発が起こるが、しだいに凝縮も起こるようになり、ついには蒸発と凝縮がつり合うようになる。その結果、容器内の気体分子の数は一定になるので圧力も一定となる。この状態を気液平衡といい、そのときの圧力を飽和蒸気圧あるいは単に蒸気圧という。蒸気圧は温度が高いほど大きく、液体の種類によって異なる。たとえば、水とエタノールの蒸気圧と温度の関係は図1のようになる。なお、蒸気圧は同じ容器に存在する他の物質の影響を受けない。
図2のような滑らかに動くピストンによって圧力に応じて容積が変化する容器がある。容器のピストンはボルトで固定することができ、栓を通して容器内を真空にしたり物質を容器内に注入したりすることができる。この容器を用いて実験1~5を順次行った。なお、実験2~4では容器内の温度を27℃に保った。
(実験1)容器内を真空にしてから、水とエタノールを等量(mol)ずつ注入して、50℃で気液平衡の状態になるようにピストンを固定した。
(実験2)容器内の温度を27℃に下げて、再び真空にした。気体Aを1.0mol注入してからピストンの固定を解除し、しばらく放置した。
(実験3)ピストンを固定してエタノールを11.5g追加し、しばらく放置した。
(実験4)再びピストンの固定を解除し、しばらく放置した。
(実験5)容器内の温度をゆっくりと27℃から80℃まで上昇させた。


- (1)下線部の理由を説明せよ。
- (2)実験1における容器内の状態について、次の中から正しい記述をすべて選び、記号で答えよ。
- a.液体からは常に気泡が発生している。
- b.エタノールの分圧は水の分圧の約2.4倍である。
- c.水とエタノールの分圧の合計は大気圧に等しい。
- d.気液平衡の状態であれば、ピストンの位置を変えても気体分子の数は変わらない。
- e.エタノールの液体分子は水の液体分子よりも少ない。
- (3)実験2の結果、気体Aの密度は0.162g/Lになった。
- (ⅰ)標準状態における気体Aの密度(g/L)を有効数字3桁で求めよ。計算の過程も示すこと。
- (ⅱ)気体Aの分子式を書け。
- (4)実験3の結果、容器内で液体として存在するエタノールの質量(g)を有効数字2桁で求めよ。計算の過程も示すこと。
- (5)実験4の結果、容器内の体積は実験3の状態の何倍になるか。次の中から最も適当なものを選び、記号で答えよ。
- a.0.80倍
- b.0.90倍
- c.1.0倍
- d.1.1倍
- e.1.2倍
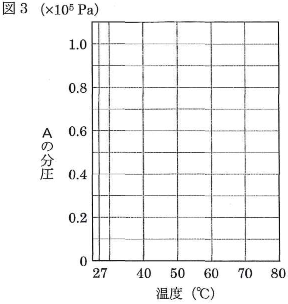
- (6)実験5における容器内の気体Aの分圧はどのように変化するか、図3に適当なグラフを書け。グラフには27℃と80℃におけるAの分圧の数値を示し、変化の特徴がわかるように描くこと。