順天堂大学化学2012年第3問
分子式が$\text{A}$、$\text{B}$、$\text{C}$で表される気体が以下のような可逆反応を示し、平衡状態に達しているとする。ただし、$\text{a}$、$\text{b}$、$\text{c}$は係数であり、$Q$は反応熱である。
\[
\text{aA}\leftrightarrows\text{bB}+\text{cC}+Q~[\text{kJ}]
\]
一定の温度条件下では、各物質の平衡時のモル濃度$\text{[A]}$、$\text{[B]}$、$\text{[C]}$の間に
\[
\dfrac{[\text{B}]^\text{b}[\text{C}]^\text{c}}{[\text{A}]^\text{a}}=Kc(Kcは濃度平衡定数)
\]
が成立する。
次の各問いに答えなさい。[解答番号$\fbox{1}$~$\fbox{6}$]
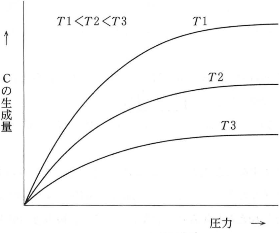
- 問1 この反応において、絶対温度$T1$、$T2$、$T3$における、圧力と平衡時の$\text{C}$の生成量の関係を図に示した。$\text{a}$、$\text{b}$、$\text{c}$、$\text{Q}$の条件として正しいものを(1)~(6)の中から一つ選びなさい。ただし、$T1\lt T2\lt T3$であるとする。$\fbox{1}$
- (1) $\text{a}\lt\text{b}+\text{c}$、$Q\lt0$
- (2) $\text{a}\lt\text{b}+\text{c}$、$Q\gt0$
- (3) $\text{a}=\text{b}+\text{c}$、$Q\lt0$
- (4) $\text{a}\gt\text{b}+\text{c}$、$Q\lt0$
- (5) $\text{a}\gt\text{b}+\text{c}$、$Q\gt0$
- (6) $\text{a}=\text{b}+\text{c}$、$Q=0$
- 問2 係数$\text{a}$、$\text{b}$、$\text{c}$がそれぞれ$\text{a}=1$、$\text{b}=2$、$\text{c}=1$であった時、温度727℃一定の条件下、真空に排気した密閉容器に気体Aを入れ、反応前の容器内の圧力を測定すると100 Paであった。その後反応が進み平衡に達した時の圧力は180 Paに変化していた。この時生成されたBの物質量は$1.00\times10^{-5}$ molであった。次の問い(a)~(e)に答えなさい。
- (a) 気体の分圧で表した平衡定数を圧平衡定数$K_p$という。モル濃度で表した濃度平衡定数$K_c$と圧平衡定数$K_p$の関係を示した正しい式を次の(1)~(6)の中から一つ選びなさい。ただし、$T$は絶対温度、$R$は気体定数である。$\fbox{2}$
- (1) $K_p=K_c$
- (2) $K_p=K_cRT$
- (3) $K_p=K_c(RT)^2$
- (4) $K_p=\dfrac{K_c}{RT}$
- (5) $K_p=\dfrac{K_c}{(RT)^2}$
- (6) $K_p=\dfrac{1}{K_c}$
- (b) 最初に入れた気体Aの物質量はいくらか。最も近い値を(1)~(6)の中から一つ選びなさい。$\fbox{3}$ mol
- (1) $0.80\times10^{-5}$
- (2) $1.00\times10^{-5}$
- (3) $1.25\times10^{-5}$
- (4) $1.80\times10^{-5}$
- (5) $2.00\times10^{-5}$
- (6) $2.50\times10^{-5}$
- (C) 平衡時の気体Aの分圧はいくらになるか。最も近い値を(1)~(6)の中から一つ選びなさい。$\fbox{4}$ Pa
- (1) 10
- (2) 60
- (3) 90
- (4) 100
- (5) 135
- (6) 180
- (d) この平衡状態に達した反応系に、体積、温度を一定のまま、新たに気体Aを加えたところ、気体Bの分圧が160 Paとなって再び平衡に達した。新たに加えた気体Aの物質量はいくらか。最も近い値を(1)~(6)の中から一つ選びなさい。$\fbox{5}$ mol
- (1) $1.25\times10^{-5}$
- (2) $2.25\times10^{-5}$
- (3) $3.75\times10^{-5}$
- (4) $5.75\times10^{-5}$
- (5) $6.25\times10^{-5}$
- (6) $8.75\times10^{-5}$
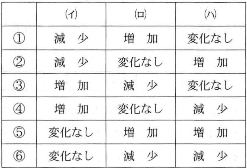
- (e) (d)での新たな平衡状態に次の(イ)~(ハ)のような変化を与えると気体Aの物質量はどうなるか。正しい組み合わせを(1)~(6)の中から一つ選びなさい。$\fbox{6}$
- (イ) 温度を一定に保ち、体積を変動させ、全圧を800 Paにする。
- (ロ) 温度、全圧を一定に保ち、アルゴンを加え、体積を2倍にする。
- (ハ) 温度、体積を一定に保ち、アルゴンを加える。
- (a) 気体の分圧で表した平衡定数を圧平衡定数$K_p$という。モル濃度で表した濃度平衡定数$K_c$と圧平衡定数$K_p$の関係を示した正しい式を次の(1)~(6)の中から一つ選びなさい。ただし、$T$は絶対温度、$R$は気体定数である。$\fbox{2}$