金沢医科大学化学2012年第1問
- (1) a~eは、1~10のいずれかの元素またはその単体についての記述である。a~eには、ある元素についての記述が2つ含まれている。その元素はどれか。$\fbox{1}$
- a.塩化ナトリウム水溶液の電気分解により得られる。
- b.3つの同素体が存在し金属銅と反応し黒色沈殿物をつくる。
- c.酸化数+2の化合物をつくり、燃焼すると白色の酸化物を生じる。
- d.塩酸、水酸化ナトリウム水溶液のいずれにも、水素を発生して溶ける。
- e.水素化物は、還元性をもち水溶液は弱酸性を示す。
- (ア) $\text{Li}$
- (イ) $\text{F}$
- (ウ) $\text{Na}$
- (エ) $\text{Mg}$
- (オ) $\text{Al}$
- (カ) $\text{Si}$
- (キ) $\text{P}$
- (ク) $\text{S}$
- (ケ) $\text{Cl}$
- (コ) $\text{Ar}$
- (2) 次の記述の中で、下線部の元素の酸化数が反応の前後で変化するものをすべて選びなさい。$\fbox{2}$
- (ア) 二酸化窒素$\underline{\text{N}}\text{O}_2$を密閉容器に入れ、温度一定のまま圧力を加える。
- (イ) 塩素$\underline{\text{Cl}}_2$を水に溶かす。
- (ウ) ヨウ素ヨウ化カリウム水溶液に硫化水素$\text{H}_2\underline{\text{S}}$を通じる。
- (エ) 酸化マンガン(IV)$\underline{\text{Mn}}\text{O}_2$に過酸化水素を加える。
- (オ) 硫酸銅(II)$\text{Cu}\underline{\text{S}}\text{O}_4$水溶液に鉄片を入れる。
- (3) 次の反応式の係数(a、b、c、d、e、fの順)で正しいものはどれか。$\fbox{3}$
\[\fbox{a}\text{KMnO}_4+\fbox{b}\text{HCl}\longrightarrow\fbox{c}\text{MnCl}_2+\fbox{d}\text{KCl}+\fbox{e}\text{H}_2\text{O}+\fbox{f}\text{Cl}_2\]
- (ア) 1、1、1、1、4、1
- (イ) 1、2、1、1、4、1
- (ウ) 1、4、1、1、2、1
- (エ) 1、4、1、1、4、1
- (オ) 2、8、2、2、4、1
- (カ) 2、8、2、2、4、3
- (キ) 1、16、1、1、8、5
- (ク) 2、16、2、2、8、3
- (ケ) 2、16、2、2、8、5
- (コ) 2、32、2、2、16、5
- (4) 濃硫酸に関するa~dの記述について、正誤の組合せ(a、b、c、dの順)として正しいものはどれか。$\fbox{4}$
- a.高い粘性をもち、不揮発性である。
- b.加熱すると強い還元作用を示す。
- c.塩化ナトリウムに加え加熱すると塩素が発生する。
- d.ショ糖を炭化させる。
- (ア) 正、正、正、正
- (イ) 誤、正、正、正
- (ウ) 正、誤、正、正
- (エ) 正、誤、正、誤
- (オ) 正、誤、誤、正
- (カ) 誤、正、正、誤
- (キ) 誤、正、誤、正
- (ク) 誤、誤、誤、正
- (ケ) 正、誤、誤、誤
- (コ) 誤、正、誤、誤
- (5) フェノールに関するa~dの記述について、正誤の組合せ(a、b、c、dの順)として正しいものはどれか。$\fbox{5}$
- a.無色で特有の臭いがあり、常温・常圧で液体である。
- b.炭酸水素ナトリウム水溶液によく溶ける。
- c.水溶液に臭素水を加えると白色沈殿を生じる。
- d.水溶液に塩化鉄(III)水溶液を加えると、黄色を呈する。
- (ア) 正、正、正、誤
- (イ) 正、正、誤、正
- (ウ) 正、誤、正、正
- (エ) 正、誤、正、誤
- (オ) 正、誤、誤、正
- (カ) 誤、正、正、誤
- (キ) 誤、正、誤、正
- (ク) 誤、誤、正、正
- (ケ) 誤、誤、誤、正
- (コ) 誤、誤、正、誤
- (6) 次の組合せで2種の物質を等量混合したとき、完全に溶け合わず2層の液体層を形成するものをすべて選びなさい。$\fbox{6}$
- (ア) アセトンとメタノール
- (イ) エタノールと水
- (ウ) グリセリンと水
- (エ) 酢酸と水
- (オ) ジエチルエーテルと水
- (カ) ベンゼンとヘキサン
- (キ) 1-ブタノールと水
- (ク) ベンゼンと水
- (ケ) メタノールと水
- (コ) ホルムアルデヒドと水
- (7) 鎖式化合物Xは分子量100のカルボン酸であり、完全燃焼させると二酸化炭素と水が物質量比5:4で生成した。Xとして推定できる化合物はいくつあるか。ただし、幾何異性体、光学異性体は区別しなくてよい。$\fbox{7}$
- (ア) 6
- (イ) 7
- (ウ) 8
- (エ) 9
- (オ) 10
- (カ) 11
- (キ) 12
- (ク) 13
- (ケ) 14
- (コ) 15
- (8) 設問(7)の化合物Xの中で、幾何異性体または光学異性体をもつ化合物はいくつあるか。$\fbox{8}$
- (ア) 1
- (イ) 2
- (ウ) 3
- (エ) 4
- (オ) 5
- (カ) 6
- (キ) 7
- (ク) 8
- (ケ) 9
- (コ) 10
- (9) 化合物A、Bは、いずれも分子式$\text{C}_9\text{H}_{16}\text{O}_4$で表される脂肪族ジエステルである。A、Bいずれの化合物も、完全に加水分解すると2種のアルコールと分子式$\text{C}_4\text{H}_6\text{O}_4$のジカルボン酸が生成する。Aから得られる2種のアルコールのうち一方はメタノールであり、もう一方のアルコールは、炭素が枝分かれした構造をもち、これを酸化すると還元性を有する化合物が生成する。Aから得られるもう1つのアルコールはどれか。$\fbox{9}$
- (ア) メタノール
- (イ) 1-プロパノール
- (ウ) 1-ブタノール
- (エ) 2-メチル-1-プロパノール
- (オ) エタノール
- (カ) 2-プロパノール
- (キ) 2-ブタノール
- (ク) 2-メチル-2-プロパノール
- (10) 設問(9)において、Bから得られる2種のアルコールは、いずれもアルカリ溶液中、ヨウ素と反応して特異なにおいをもつ黄色の沈殿を生成する。Bから得られる2種のアルコールを、解答群から選びなさい。$\fbox{10}$
- (ア) メタノール
- (イ) 1-プロパノール
- (ウ) 1-ブタノール
- (エ) 2-メチル-1-プロパノール
- (オ) エタノール
- (カ) 2-プロパノール
- (キ) 2-ブタノール
- (ク) 2-メチル-2-プロパノール
- (11) 炭素、水素、酸素からなる有機化合物4.8 mgを$\text{CuO}$と$\text{O}_2$存在下で十分加熱した。加熱後に生じた気体すべてを、塩化カルシウムが充てんされたガラス管、続いてソーダ石灰が充てんされたガラス管に通した。気体通過後、塩化カルシウム管の質量は2.88 mg、ソーダ石灰管の質量は7.04 mg増加していた。また、この化合物9.0 gを水100 gに溶解した水溶液の凝固点は$-0.925\ {}^\circ\mathrm{C}$であった。この化合物の分子式を求めると、$\text{C}_{\fbox{11}\fbox{12}}\text{H}_{\fbox{13}\fbox{14}}\text{O}_{\fbox{15}\fbox{16}}$である。$\fbox{11}$~$\fbox{16}$に入る数字として適するものを選びなさい。なお、$\text{C}_4$のような場合は、$\fbox{0}$$\fbox{4}$と選択しなさい。
- (ア) 1
- (イ) 2
- (ウ) 3
- (エ) 4
- (オ) 5
- (カ) 6
- (キ) 7
- (ク) 8
- (ケ) 9
- (コ) 0
- (12) ヒトの血液の浸透圧は塩化ナトリウム9.0 gを水に溶かして1 Lとした水溶液と等しい。ヒト血液と同温で同浸透圧のスクロース水溶液を1 Lつくるのに必要なスクロースは何 gか。最も近い値を選びなさい。$\fbox{17}$
- (ア) 9
- (イ) 18
- (ウ) 25
- (エ) 28
- (オ) 50
- (カ) 53
- (キ) 55
- (ク) 105
- (ケ) 110
- (コ) 180
- (13) 文章中の下線部(a)~(i)のうち、誤っている箇所をすべて選びなさい。$\fbox{18}$ デンプンは、$\alpha$-グルコースが(a)付加重合した(b)多糖類で、分子式(c)$\underline{(\text{C}_6\text{H}_{12}\text{O}_6)_n}$で表され、 穀類やイモ類などに多く含まれる。食物中のデンプンは、だ液中の(d)アミラーゼで(e)加水分解され、デキストリンを経て(f)マルトースになる。さらに膵臓の消化液中の酵素によってグルコースまで分解される。グルコースは小腸から吸収され、一部は肝臓や筋肉で(g)アミロペクチンになり蓄えられる。他のグルコースは血液を通じて各組織の細胞に運ばれ、(h)酸化されて二酸化炭素と水になる。この過程で放出されるエネルギーが運動や体温の維持、物質の合成などに利用される。肝臓の(g)アミロペクチンは必要に応じて分解されて、(A)血液中のグルコース濃度を一定(0.1%:質量パーセント濃度)に保つのに寄与している。血液中のグルコース濃度を一定に保つ機構に狂いが生じ、常に(i)低い状態になっているのが糖尿病である。
- (14) 設問(13)の下線部(A)において、血液中のグルコースのモル濃度を求めると、$\fbox{19}$、$\fbox{20}\times10^{-\fbox{21}}\text{mol}/\text{L}$となる。ただし、血液は完全な液体とし、密度は$1.02\text{g}/\text{cm}^3$とする。
$\fbox{19}$~$\fbox{21}$に入る数字として適するものを選びなさい。
- (ア) 1
- (イ) 2
- (ウ) 3
- (エ) 4
- (オ) 5
- (カ) 6
- (キ) 7
- (ク) 8
- (ケ) 9
- (コ) 0
- (15) 水溶液中のリン酸は次のように三段階で電離する。
\[\text{(第一段階の電離)}~~\text{H}_3\text{PO}_4\leftrightarrows\text{H}_2\text{PO}_4~^-+\text{H}^+~~K_1=7.1\times10^{-3}\text{mol}/\text{L}\]
\[\text{(第二段階の電離)}~~\text{H}_2\text{PO}_4~^-\leftrightarrows\text{H}\text{PO}_4~^{2-}+\text{H}^+~~K_2=6.3\times10^{-8}\text{mol}/\text{L}\]
\[\text{(第三段階の電離)}~~\text{H}\text{PO}_4~^{2-}\leftrightarrows\text{PO}_4~^{3-}+\text{H}^+~~K_3=4.5\times10^{-13}\text{mol}/\text{L}\]
ここで、$K$、$K_2$、$K_3$はリン酸の第一段階、第二段階および第三段階の電離定数とする。水溶液中の$\text{H}_3\text{PO}_4$、$\text{H}_2\text{PO}_4~^-$、$\text{H}\text{PO}_4~^{2-}$および$\text{PO}_4~^{3-}$の存在比は、水溶液のpHによって異なる。
濃度$c~\text{mol}/\text{L}$のリン酸水溶液のpHを測定したところ、2.0であった。このリン酸水溶液では、第二段階、第三段階の電離は無視でき、第一段階における電離平衡のみを考えればよいので、$[\text{H}^+]=[\text{H}_2\text{PO}_4~^-]$とみなせる。ただし、このときの電離度$\alpha$は1に対して無視できない。これらのことを考慮して、電離度$\alpha$を求めると、$\alpha$は$0.\fbox{22}\fbox{23}$となり、リン酸水溶液の濃度$c$を求めると、$c$は$\fbox{24}.\fbox{25}\times10^{-\fbox{26}}\text{mol}/\text{L}$となる。
$\fbox{22}$~$\fbox{26}$に入る数字として適するものを選びなさい。
- (ア) 1
- (イ) 2
- (ウ) 3
- (エ) 4
- (オ) 5
- (カ) 6
- (キ) 7
- (ク) 8
- (ケ) 9
- (コ) 0
- (16) 次の物質の結晶のうち、分子結晶を3つ選びなさい。$\fbox{27}$
- (ア) アルミニウム
- (イ) カルシウム
- (ウ) ベンゼン
- (エ) ヨウ素
- (オ) 塩化セシウム
- (カ) 黒鉛
- (キ) 酸化マグネシウム
- (ク) 二酸化ケイ素
- (ケ) 二酸化炭素
- (コ) 炭酸カルシウム
- (17)放射性同位体は不安定で、原子核が放射線($\alpha$線はヘリウム原子核、$\beta$線は電子)を放出して別の原子に変化する。放射性同位体$^{235}_{92}\text{U}$が$\alpha$線を放出して崩壊した場合、および$^{14}_6\text{C}$が$\beta$線を放出して崩壊した場合、それぞれに当てはまるものをすべて選びなさい。解答棚は$^{235}_{92}\text{U}$については$\fbox{28}$、$^{14}_6\text{C}$については$\fbox{29}$を使用しなさい。
- (ア) 原子番号不変
- (イ) 原子番号1増加
- (ウ) 原子番号2増加
- (エ) 原子番号1減少
- (オ) 原子番号2減少
- (カ) 質量数不変
- (キ) 質量数1減少
- (ク) 質量数2減少
- (ケ) 質量数3減少
- (コ) 質量数4減少
- (18)過酸化水素水に塩化鉄(III)を少量加えると、分解反応が開始され酸素が発生した。分解反応開始後の過酸化水素量と発生した酸素量を図に表した。図中、ある時点$t$での物質量$a$と$b$の比$(a:b)$について正しいのはどれか。$\fbox{30}$
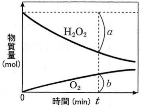
- (ア) 最初の過酸化水素濃度により変わる
- (イ) 加える塩化鉄の量により変わる
- (ウ) 1:1で一定
- (エ) 2:1で一定
- (オ) 3:1で一定
- (カ) 4:1で一定
- (キ) 反応開始当初は1:1だが徐々に2:1に近づく
- (ク) 反応開始当初は2:1だが徐々に1:1に近づく
- (ケ) 反応開始当初は2:1だが徐々に$b$の比が大きくなる
- (コ) 反応開始当初は2:1だが徐々に$b$の比が小さくなる
- (19) 設問(18)において、ある条件で分解反応を開始し、時間ごとの過酸化水素
濃度を実際に測定した結果を表に示した。
このとき、2.0~4.0 minの間の酸素の発生速度は$\fbox{31}.\fbox{32}\times10^{-\fbox{33}}\text{mol}/\text{L}\cdot\text{min}$である。 $\fbox{31}$~$\fbox{33}$に入る数字として適するものを選びなさい。反応時間[min] 0 1.0 2.0 3.0 4.0 5.0 6.0 $\text{H}_2\text{O}_2$濃度[$\times10^{-2}\text{mol}/\text{L}$] 2.57 2.44 2.33 2.23 2.15 2.08 2.02 - (ア) 1
- (イ) 2
- (ウ) 3
- (エ) 4
- (オ) 5
- (カ) 6
- (キ) 7
- (ク) 8
- (ケ) 9
- (コ) 0
- (20) 設問18において、塩化鉄(III)より分解効果が大きい酸化マンガン(IV)を加えた場合、グラフはどうなるか。$\fbox{34}$