川崎医科大学化学2013年第1問
各問いに答えよ。
- [1] 下線部が単体の意味で用いられているのはどれか。一つ選べ。$\fbox{ア}$
- (1)火山地帯の温泉には硫黄の臭いがするところがある。
- (2)金魚は水中の酸素を鰓から血液に取り入れている。
- (3)肥料の中にはカリウムを含むものがある。
- (4)骨にはカルシウムが含まれている。
- (5)水の質量の約11%が水素である。
- [2] a~cのそれぞれについて、含まれる電子の総数が多い順に並んでいるのはどれか。一つ選べ。$\fbox{イ}$
【電子の総数の例】1.0molのヘリウムに含まれる電子の総数は$1.2\times10^{24}$個である。- $a$ 3.6gの水
- $b$ 標準状態で4.48Lの水素
- $c$ 0.1mo1のナトリウムイオン
- (1)$a\gt b\gt c$
- (2)$a\gt c\gt b$
- (3)$b\gt a\gt c$
- (4)$b\gt c\gt a$
- (5)$c\gt a\gt b$
- (6)$c\gt b\gt a$
- [3] ある金属Mの酸化物$w$〔g〕中に、Mが$m$〔g〕含まれている。Mの原子量を求めるとき、$w$と$m$以外に、次の値や式のうち必要なのはどれか。正しい組合せを一つ選べ。$\fbox{ウ}$
アボガドロ定数 酸素の原子量 酸化物の組成式 (1) 必要 必要 必要 (2) 必要 必要 不要 (3) 必要 不要 必要 (4) 必要 不要 不要 (5) 不要 必要 必要 (6) 不要 必要 不要 (7) 不要 不要 必要 (8) 不要 不要 不要 - [4] 次の熱化学方程式から、エチレンの生成熱(kJ/mol)を求めよ。$\fbox{エ}$には+または-の符号を、$\fbox{オ}$~$\fbox{キ}$には数値を入れよ。$\fbox{エ}$$\fbox{オ}$$\fbox{カ}$$\fbox{キ}$kJ/mol
- $\text{C}(黒鉛)+\text{O}_2(気)=\text{CO}_2(気)+394\text{kJ}$
- $\text{H}_2(気)+\dfrac{1}{2}\text{O}_2(気)=\text{H}_2\text{O}(液)+286\text{kJ}$
- $\text{C}_2\text{H}_4(気)+3\text{O}_2(気)=2\text{CO}_2(気)+2\text{H}_2\text{O}(液)+1411\text{kJ}$
- [5] 反応により、下線部の原子の酸化数が減少しているのはどれか。一つ選べ。$\fbox{ク}$
- (1)$\text{K}_2\underline{\text{Cr}}_2\text{O}_7+2\text{KOH}\rightarrow2\text{K}_2\underline{\text{Cr}}\text{O}_4+\text{H}_2\text{O}$
- (2)$2\text{KMnO}_4+5\underline{\text{S}}\text{O}_2+2\text{H}_2\text{O}\rightarrow2\text{MnSO}_4+\text{K}_2\underline{\text{S}}\text{O}_4+2\text{SO}_4$
- (3)$\text{Cu}+4\text{H}\underline{\text{N}}\text{O}_3\rightarrow\text{Cu}(\underline{\text{N}}\text{O}_3)_2+2\text{NO}_2+2\text{H}_2\text{O}$
- (4)$\text{K}_2\underline{\text{Cr}}_2\text{O}_7+3\text{H}_2\text{O}_2+4\text{H}_2\text{SO}_4\rightarrow\underline{\text{Cr}}_2(\text{SO}_4)_3+3\text{O}_2+7\text{H}_2\text{O}+\text{K}_2\text{SO}_4$
- (5)$2\text{H}_2\underline{\text{O}}_2\rightarrow2\text{H}_2\text{O}+\underline{\text{O}}_2$
- (6)$2\text{K}\underline{\text{I}}+\text{Cl}_2\rightarrow2\text{KCl}+\underline{\text{I}}_2$
- [6] [ ]には「酸」または「塩基」の語が入る。$\fbox{A}$、$\fbox{B}$および$\fbox{C}$に入る語の組合せで正しいのはどれか。一つ選べ。$\fbox{ケ}$
ブレンステッド・ローリーの定義によると、[ ]とは水素イオンを相手に与える物質のことをいい、$\fbox{A}$とは水素イオンを受け取る物質のことをいう。この定義によると、水はアンモニアと反応するとき、$\fbox{B}$として働く。
また、弱酸の塩または弱塩基の塩を水に溶解すると、塩が電離して生じたイオンが水分子と反応して、水溶液中に水酸化物イオンまたは水素イオンが増える。たとえば、塩化アンモニウムの水溶液では、電離で生じたアンモニウムイオンの一部が水と反応するので、水溶液は弱い$\fbox{C}$性を示す。
A B C (1) 塩基 塩基 塩基 (2) 塩基 塩基 酸 (3) 塩基 酸 塩基 (4) 塩基 酸 酸 (5) 酸 塩基 塩基 (6) 酸 塩基 酸 (7) 酸 酸 塩基 (8) 酸 酸 酸 - [7] 硝酸銅(Ⅱ)と硝酸銀(Ⅰ)の両方が溶けた水溶液がある。銅(Ⅱ)イオンと銀(Ⅰ)イオンの一方のみを沈殿物にする操作はどれか。一つ選べ。$\fbox{コ}$
- (1)過剰量の塩酸を加える。
- (2)過剰量のアンモニア水を加える。
- (3)溶液を塩基性にして硫化水素を通じる。
- (4)溶液を酸性にして硫化水素を通じる。
- (5)過剩量の水酸化ナトリウム水溶液を加える。
- [8] 次の文を読み、問いに答えよ。
鉛蓄電池は負極に鉛、正極に酸化鉛(Ⅳ)、電解液に希硫酸を用いた二次電池である。放電時には、負極、正極のそれぞれで次の反応が起きている。
- 負極:$\text{Pb}+\text{SO}_4{^{2-}}\rightarrow\text{PbSO}_4+2\text{e}^-$
- 正極:$\text{PbO}_2+\text{SO}_4{^{2-}}+4\text{H}^++2\text{e}^-\rightarrow\text{PbSO}_4+2\text{H}_2\text{O}$
- 1)放電により生じた硫酸鉛(Ⅱ)(モル質量303g/mol)の質量は、両極あわせて何gか。数値を入れよ。$\fbox{サ}$$\fbox{シ}$g
- 2)放電により、電解液の密度とpHはそれぞれどのようになるか。正しい組合せを一つ選べ。$\fbox{ス}$
電解液の密度 電解液のpH (1) 増加する 増加する (2) 増加する 変化しない (3) 増加する 減少する (4) 変化しない 増加する (5) 変化しない 変化しない (6) 変化しない 減少する (7) 減少する 増加する (8) 減少する 変化しない (9) 減少する 減少する
- [9] 誤っているのはどれか。一つ選べ。$\fbox{セ}$
- (1)2-ブテンにはシス-トランス異性体がある。
- (2)アセチレンは三重結合を一つもつ直線状の分子である。
- (3)アルカンには枝分かれした構造をもつものがある。
- (4)アルケンとシクロアルカンの一般式はともに$\text{C}_n\text{H}_{2n}$で表される。
- (5)メタンに塩素を反応させてクロロメタンが生成する反応は付加反応である。
- [10] 次の文を読み、問いに答えよ。
芳香族化合物AとBは炭素、水素、酸素原子からなり、互いに構造異性体の関係にある。
AとBの元素分析値は質量パーセントで炭素77.8%、水素7.4%であり、分子量は100から140の間であった。
AとBはともにナトリウムと反応して水素を発生した。
AとBが溶けているジエチルエーテル溶液に水酸化ナトリウム水溶液を加えて抽出操作を行った。エーテル層からはAが得られ、塩基性の水層からはBが得られた。
- 1)化合物AとBの分子式はどれか。一つ選べ。$\fbox{ソ}$
- (1)$\text{C}_7\text{H}_6\text{O}$
- (2)$\text{C}_7\text{H}_6\text{O}_2$
- (3)$\text{C}_7\text{H}_6\text{O}_3$
- (4)$\text{C}_7\text{H}_8\text{O}$
- (5)$\text{C}_8\text{H}_8\text{O}_2$
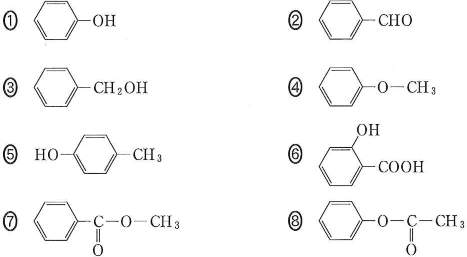
- 2)化合物Aの構造式はどれか。一つ選べ。$\fbox{タ}$
- 3)化合物AとBのそれぞれに塩化鉄(Ⅲ)水溶液を加えたとき、呈色反応が見られるのはどれか。また、$o-$、$m-$、$p-$の構造異性体をもつ化合物はどれか。正しい組合せを一つ選べ。$\fbox{チ}$
塩化鉄(Ⅲ)水溶液を加えると
呈色反応が見られる$o-$、$m-$、$p-$の構造異性体
をもつ(1) Aのみ Aのみ (2) Aのみ AとB (3) AとB Aのみ (4) AとB Bのみ (5) Bのみ AとB (6) Bのみ Bのみ
- 1)化合物AとBの分子式はどれか。一つ選べ。$\fbox{ソ}$
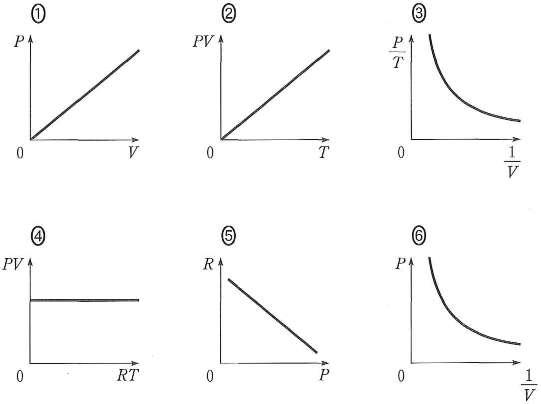
- [11] 次のグラフの縦軸と横軸の関係が、理想気体の状態方程式$PV=nRT$を正しく表しているのはどれか。一つ選べ。ただしグラフに記載のない変数は一定とし、$P$は圧力、$V$は体積、$n$は物質量、$R$は気体定数、$T$は絶対温度を表すものとする。$\fbox{ツ}$
- [12] $\fbox{テ}$~$\fbox{ニ}$に、最も適切なものを一つずつ選べ。
化合物Xは$\fbox{テ}$、化合物Yは$\fbox{ト}$である。これらが$\fbox{ナ}$結合で重合してできた高分子化合物を$\fbox{ニ}$という。
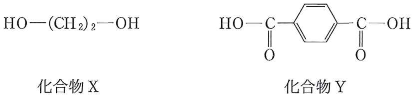
- $\fbox{テ}$、$\fbox{ト}$の選択肢
- (1)酢酸エチル
- (2)サリチル酸
- (3)テレフタル酸
- (4)クレゾール
- (5)酢酸ビニル
- (6)アジピン酸
- (7)エチレングリコール
- $\fbox{ナ}$の選択肢
- (1)アミド
- (2)イオン
- (3)エステル
- (4)エーテル
- (5)ペプチド
- $\fbox{ニ}$の選択肢
- (1)ビニロン
- (2)ポリエチレンテレフタラート
- (3)絹
- (4)アセテート
- (5)ナイロン66
- $\fbox{テ}$、$\fbox{ト}$の選択肢
- [13] 次の物質のうち、4種類以上の元素を含む物質はどれか。二つ選び、$\fbox{ヌ}$に二つマークせよ。$\fbox{ヌ}$
- (1)アデノシン三リン酸
- (2)デンプン
- (3)ナイロン6
- (4)ポリ塩化ビニル
- (5)リボース