福岡大学化学2012年第3問
ガスボンベ中の混合気体の平均分子量とその組成を求めるために、次の実験を行った(図1参照)。このときの温度$(t)$は27℃、大気圧$(p)$は103.60kPaであった。
実験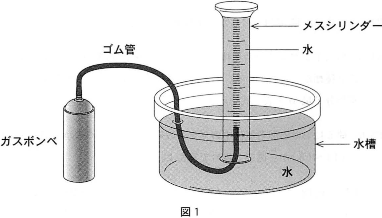
実験
- 1 混合気体の入ったガスボンベの質量$w_1$を測定したところ、198.18gであった。
- 2 ガスボンベにゴム管をつなぎ、水を満たしたメスシリンダーを水槽に倒立させた装置を組み立てた(図1)。
- 3 ガスボンベから気体の一部を放出し、そのすべてをメスシリンダーに捕集した。その後、ゴム管をメスシリンダーから取り除いた。
- 4 メスシリンダーの水面と水槽の水面を一致させ、気体の体積$v$を測定したところ、450mLであった。
- 5 ガスボンベからゴム管を取り外し、ガスボンベの質量$w_2$を測定したところ、197.18gであった。
次の問1~問6に答えよ。
ただし、気体は理想気体とし、気体の水への溶解およびゴム管内の気体の量は無視できるものとする。また気体定数は$R=8.31\times10^3~\text{L}\cdot\text{Pa}/(\text{K}\cdot\text{mol})$とし、27℃における水の飽和蒸気圧は$p_{\text{H}_2\text{O}}=3.60~\text{kPa}$とする。

- 問1 飽和蒸気圧に関する次の記述(1)~(5)のうち、正しいものを選び、番号で答えよ。
- (1) 温度が高くなるほど飽和蒸気圧は小さくなる。
- (2) 一定温度のもとで、他の気体が存在すると飽和蒸気圧は小さくなる。
- (3) 一定温度のもとでは、分子間力の強い液体ほど飽和蒸気圧は大きい。
- (4) 沸点における飽和蒸気圧は大気圧と等しい。
- (5) 一定温度のもとで、不揮発性の物質を溶かすと飽和蒸気圧は大きくなる。
- 問2 ガスボンベから放出された混合気体の物質量は$v$、$t$、$p$、$p_{\text{H}_2\text{O}}$、$R$を用いるとどのように表わせるか。下の(1)~(8)から正しいものを選び、番号で答えよ。
- (1) $\dfrac{(p+p_{\text{H}_2\text{O}})v}{R(273+t)}$
- (2) $\dfrac{(p-p_{\text{H}_2\text{O}})v}{R(273+t)}$
- (3) $\dfrac{(p+p_{\text{H}_2\text{O}})v}{Rt}$
- (4) $\dfrac{(p-p_{\text{H}_2\text{O}})v}{Rt}$
- (5) $\dfrac{R(273+t)}{(p+p_{\text{H}_2\text{O}})v}$
- (6) $\dfrac{R(273+t)}{(p-p_{\text{H}_2\text{O}})v}$
- (7) $\dfrac{Rt}{(p+p_{\text{H}_2\text{O}})v}$
- (8) $\dfrac{Rt}{(p-p_{\text{H}_2\text{O}})v}$
- 問3 混合気体の平均分子量を$M$として、ガスボンベから放出された混合気体の物質量を$M$、$w_1$、$w_2$を用いて表わせ。
- 問4 平均分子量$M$はいくらか。小数第1位まで答えよ。
- 問5 ガスボンベ中の混合気体には、ブタン(分子量58)とプロパン(分子量44)の2種類が含まれている。この混合気体中のブタンのモル分率を$x$として、平均分子量$M$を表す式を示せ。
- 問6 問5における混合気体中のブタンのモル分率はいくらか。最も近い値を次の(1)~(6)から選び、番号で答えよ。
- (1) 0.19
- (2) 0.36
- (3) 0.44
- (4) 0.56
- (5) 0.64
- (6) 0.81