北里大学化学2013年第1問
次の[1]~[8]の問に答えよ。答は各問の(1)から始まる選択肢の中から選べ。
- [1]カルシウムの化合物に関する次の記述のうちから、誤っているものを2つ選べ。$\fbox{1}$
- a.塩化カルシウムの無水塩は、空気中で潮解する。
- b.炭酸カルシウムが塩酸と反応すると、二酸化炭素が発生する。
- c.硫酸カルシウム二水和物を焼くことにより得られる焼きセッコウは、無水塩である。
- d.酸化カルシウムが水と反応すると、消石灰が生じる。
- e.水酸化カルシウム水溶波に二酸化炭素を通じると、炭酸水素カルシウムの沈般が生じる。
- (1)a、b
- (2)a、c
- (3)a、d
- (4)a、e
- (5)b、c
- (6)b、d
- (7)b、e
- (8)c、d
- (9)c、e
- (10)d、e
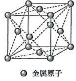
- [2]ある金属(モル質量$M$〔g/mol〕)の結晶構造は、右図のような面心立方格子である。この結晶の密度が$d$〔g/cm3〕、単位格子の一辺の長さが$l$〔cm〕であるとき、アボガドロ定数〔/mol〕を表す式はどれか。$\fbox{2}$
- (1)$\dfrac{2M}{dl^3}$
- (2)$\dfrac{dl^3}{2M}$
- (3)$\dfrac{M}{2dl^3}$
- (4)$\dfrac{2dl^3}{M}$
- (5)$\dfrac{4M}{dl^3}$
- (6)$\dfrac{dl^3}{4M}$
- (7)$\dfrac{M}{4dl^3}$
- (8)$\dfrac{4dl^3}{M}$
- [3]エタンとグラファイトをそれぞれ完全燃焼させたところ、発生した熱量は等しかった。このとき、エタンの燃焼で発生した二酸化炭素の物質量は、グラファイトの燃焼で発生した二酸化炭素の物質量の何倍か。最も近いものを選べ。ただし、水(液体)、二酸化炭素、エタンの生成熱を、それぞれ286kJ/mol、394kJ/mol、84kJ/molとする。$\fbox{3}$
- (1)0.31
- (2)0.50
- (3)0.62
- (4)1.0
- (5)1.6
- (6)2.0
- (7)3.2
- (8)4.0
- [4]金は、硝酸や熱濃硫酸には溶けないが、濃硝酸と濃塩酸を1:3の体積比で混合した溶液である王水には溶ける。王水中では、硝酸と塩酸の一部が$\eqref{aa}$式のように反応し、塩素と塩化ニトロシル$\text{NOCl}(\text{O}=\text{N}-\text{Cl})$が生じている塩化ニトロシル中の塩素原子の酸化数は-1である。
\[\text{HNO}_3+3\text{HCl}\longrightarrow\text{Cl}_2+\text{NOCl}+2\text{H}_2\text{O}\tag{1}\label{aa}\]
王水に金を浸すと、金は$\eqref{ab}$式のように塩化物イオンを配位子とする錯イオンを形成して溶ける。
\[\text{Au}+\text{NOCl}+\text{Cl}_2+\text{HCl}\longrightarrow[\text{AuCl}_4]^-+\text{H}^++\text{NO}\tag{2}\label{ab}\]
$\eqref{ab}$式で酸化剤として働く物質はどれか。$\fbox{4}$
- (1)$\text{Au}$のみ
- (2)$\text{NOCl}$のみ
- (3)$\text{Cl}_2$のみ
- (4)$\text{HCl}$のみ
- (5)$\text{Au}$と$\text{NOCl}$
- (6)$\text{Au}$と$\text{Cl}_2$
- (7)$\text{Au}$と$\text{HCl}$
- (8)$\text{NOCl}$と$\text{Cl}_2$
- (9)$\text{NOCl}$と$\text{HCl}$
- (10)$\text{Cl}_2$と$\text{HCl}$
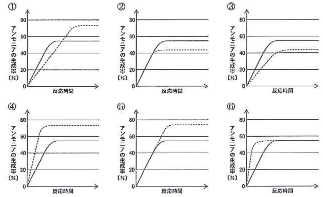
- [5]窒素と水素からアンモニアが生成する反応は可逆反応である。触媒を加えずに、一定圧力、一定温度で窒素と水素を反応させると、アンモニアの生成率(%)は反応時間とともに図中の実線のように変化した。触媒を加え、他の条件を同じにして窒素と水素を反応させたときのアンモニアの生成率と反応時間の関係を破線で表した図はどれか。$\fbox{5}$
- [6]次の記述のうちから、正しいものを2つ選べ。$\fbox{6}$
- a.デンプン2.0gを水1Lに溶かした水溶液の60℃での浸透圧は、同じ水溶液の20℃での浸透圧より小さい。
- b.デンプン水溶液の入ったセロハン膜の袋を水に浸し放置すると、袋の中の水溶液の体積は増加する。
- c.0.10mol/kgグルコース水溶液の凝固点は、0.20mol/kgグルコース水溶液の凝固点より低い。
- d.0.10mol/kgグルコース水溶液の沸点は、0.10mol/kgスクロース水溶液の沸点より低い。
- e.0.10mol/kg塩化カルシウム水溶液の90℃での蒸気圧は、0.10mol/kg硝酸カリウム水溶液の90℃での蒸気圧より低い。
- (1)a、b
- (2)a、c
- (3)a、d
- (4)a、e
- (5)b、c
- (6)b、d
- (7)b、e
- (8)c、d
- (9)c、e
- (10)d、e
- [7]炭素数が3である有機化合物に関する次の記述のうちから、正しいものを2つ選べ。$\fbox{7}$
- a.プロペン(プロピレン)1分子には、臭素2分子が付加する。
- b.プロピンの3つの炭素原子は、一直線上にない。
- c.1-プロパノールとエチルメチルエーテルは、互いに構造異性体である。
- d.2-プロパノールとアセトンは、いずれもヨードホルム反応を呈する。
- e.1-プロパノールと2-プロパノールをそれぞれ酸化剤で酸化して得られる化合物は、いずれも銀鏡反応を呈する。
- (1)a、b
- (2)a、c
- (3)a、d
- (4)a、e
- (5)b、c
- (6)b、d
- (7)b、e
- (8)c、d
- (9)c、e
- (10)d、e
- [8]アニリン、安息香酸、$p$-キシレン、フェノールをジエチルエーテルに溶解した混合溶液がある。下図のステップ1およびステップ2において、下記の操作(ア)あるいは(イ)を行うと、各化合物を水層あるいはエーテル層に分離することができる。方法Aでは、ステップ1で操作(ア)を行い、ステップ2で操作(イ)を行う。方法Bでは、逆に、ステップ1で操作(イ)を行い、ステップ2で操作(ア)を行う。次の記述のうちから、正しいものを2つ選べ。$\fbox{8}$
操作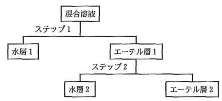
- (ア)希塩酸と振り混ぜ、水層とエーテル層を分離する。
- (イ)炭酸水素ナトリウム水溶波と振り混ぜ、水層とエーテル属を分離する。
- a.方法Aでも方法Bでも、分液漏斗で混合溶液をよく振り静置すると、上層は水層、下層はエーテル層となる。
- b.方法Aでは、アニリンは水層1に、安息香酸は水層2に抽出される。
- c.方法Bでは、フェノールは水層1に、アニリンは水層2に抽出される。
- d.方法Aでも方法Bでも、アニリンは水層1または水層2のいずれかに抽出される。水層からアニリンを遊離させるには、水酸化ナトリウム水溶液を加えるとよい。
- e.方法Aでも方法Bでも、$p$-キシレンはエーテル層に残る。このエーテル層から、$p$-キシレンを分離するには、エーテル層を濃縮し、氷中で冷却するとよい。
- (1)a、b
- (2)a、c
- (3)a、d
- (4)a、e
- (5)b、c
- (6)b、d
- (7)b、e
- (8)c、d
- (9)c、e
- (10)d、e