杏林大学化学2013年第3問
次の文章を読み、問いに答えよ。[解答欄$\fbox{ア}$~$\fbox{ソ}$]
- 問1 シリンダーとピストンからなる装置があり、気体の体積が変わるとピストンの位置がスムースに移動するようになっている。

理想気体である$\text{A}_3\text{B}_6$は、常温付近で、解離して理想気体$\text{AB}_2$を生じ、次のように平衡を保って混合気体になる。
\[\text{A}_3\text{B}_6\rightleftarrows3\text{AB}_2\]実験1:純粋な理想気体$\text{A}_3\text{B}_6$$n$ molをシリンダーに入れ、温度27℃、圧力$1.0\times10^5$Paの状態に保ち放置した。
実験2:実験1の後、温度27℃に保ったまま、気体の体積が半分になる位置までピストンを移動させた。
- [1] 実験1で$\text{A}_3\text{B}_6$をシリンダーに入れ、十分に時間が経過した後、ピストンの位置は、$\text{A}_3\text{B}_6$を入れた直後と比べてどうなったか。最も適切なものを次の(1)~(3)の中から一つ選べ。$\fbox{ア}$
- (1)上に移動した
- (2)下に移動した
- (3)かわらなかった
- [2] 実験1で十分に時間が経過した後、各物質のモル濃度を$[\text{A}_3\text{B}_6]$、$[\text{AB}_2]$と表すと、濃度平衡定数$K_c$はどう示されるか。最も適切なものを次の(1)~(9)の中から一つ選べ。$\fbox{イ}$
- (1)$\dfrac{3[\text{AB}_2]}{[\text{A}_3\text{B}_6]}$
- (2)$\dfrac{27[\text{AB}_2]}{[\text{A}_3\text{B}_6]}$
- (3)$\dfrac{3[\text{AB}_2]^2}{[\text{A}_3\text{B}_6]}$
- (4)$\dfrac{[\text{AB}_2]^3}{[\text{A}_3\text{B}_6]}$
- (5)$\dfrac{9[\text{AB}_2]^3}{[\text{A}_3\text{B}_6]}$
- (6)$\dfrac{27[\text{A}_3\text{B}_6]}{[\text{AB}_2]}$
- (7)$\dfrac{3[\text{A}_3\text{B}_6]}{[\text{AB}_2]^2}$
- (8)$\dfrac{[\text{A}_3\text{B}_6]}{[\text{AB}_2]^3}$
- (9)$\dfrac{9[\text{A}_3\text{B}_6]}{[\text{AB}_2]^3}$
- [3] 実験1での解離度(分解した割合)を$α(0\leqq a\leqq 1)$、気体の体積を$V$ Lとする。解離度と気体の体積を用いて、濃度平衡定数$K_c$はどのように表せるか。最も適切なものを次の(1)~(9)の中から一つ選べ。$\fbox{ウ}$
- (1)$\dfrac{6α^3V^2}{1+α}$
- (2)$\dfrac{9α^3n}{(1+α)V^2}$
- (3)$\dfrac{3αn}{(1+2α)V}$
- (4)$\dfrac{27α^3V}{(1+2α)n}$
- (5)$\dfrac{α^3V}{(1+α)n^2}$
- (6)$\dfrac{9α}{(1-α)^3nV^2}$
- (7)$\dfrac{27α^3n^2}{(1-α)V^2}$
- (8)$\dfrac{3α^2n}{(1-α)V}$
- (9)$\dfrac{3αV}{(1-2α)^3n^2}$
- [4] 実験1での$\text{A}_3\text{B}_6$の分圧$P_{A3B6}$、$\text{AB}_2$の分圧$P_{AB2}$の値は、αを用いるとどのように表せるか。$\fbox{エ}$、$\fbox{オ}$に最も適切な式を下記のそれぞれの(1)~(9)の中から一つずつ選べ。
\[P_{A3B6}=\fbox{エ}\times10^5\text{Pa}\]
\[P_{AB2}=\fbox{オ}\times10^5\text{Pa}\]
$\fbox{エ}$
- (1)$\dfrac{1-α}{α}$
- (2)$\dfrac{1+2α}{2α}$
- (3)$\dfrac{1-α}{2α}$
- (4)$\dfrac{3α}{1-2α}$
- (5)$\dfrac{α}{1-2α}$
- (6)$\dfrac{1-α}{1+α}$
- (7)$\dfrac{1-α}{1+2α}$
- (8)$\dfrac{α}{1+2α}$
- (9)$\dfrac{1-2α}{1+2α}$
- (1)$\dfrac{1+2α}{α}$
- (2)$\dfrac{1-α}{2α}$
- (3)$\dfrac{1+α}{2α}$
- (4)$\dfrac{3α+1}{1-2α}$
- (5)$\dfrac{α-1}{1-2α}$
- (6)$\dfrac{2α}{1+α}$
- (7)$\dfrac{1-2α}{1+2α}$
- (8)$\dfrac{3α}{1+2α}$
- (9)$\dfrac{2α-1}{1+2α}$
- [5] 気体反応の場合は、濃度より圧力の方が測定しやすいため、反応に関わる気体の分圧で計算される圧平衡定数$K_p$が用いられる。実験1の圧平衡定数$K_p$はどのように表せるか。最も適切なものを次の(1)~(9)の中から一つ選べ。$\fbox{カ}$
- (1)$\dfrac{9α^3(1+2α)}{(1-α)^2\times10^{10}}$
- (2)$\dfrac{9(1+2α)\times10^5}{α(1-α)^2}$
- (3)$\dfrac{27(1+2α)^2}{α^3(1-α)\times10^5}$
- (4)$\dfrac{(1+α)(1-2α)^2}{3α^3\times10^{15}}$
- (5)$\dfrac{(1-α)(1-2α)\times10^{10}}{6α^2}$
- (6)$\dfrac{(1-α)^3(1+2α)^2\times10^5}{9α}$
- (7)$\dfrac{3α^3(1-α)\times10^5}{(1+2α)^2}$
- (8)$\dfrac{9α}{(1-α)(1+2α)^2\times10^{15}}$
- (9)$\dfrac{27α^3\times10^{10}}{(1-α)(1+2α)^2}$
- [6] 実験2の解離度αの値は実験1と比べてどうなったか。次の(1)~(3)の中から最も適切なものを一つ選べ。$\fbox{キ}$
- (1)小さくなった
- (2)大きくなった
- (3)かわらなった
- [1] 実験1で$\text{A}_3\text{B}_6$をシリンダーに入れ、十分に時間が経過した後、ピストンの位置は、$\text{A}_3\text{B}_6$を入れた直後と比べてどうなったか。最も適切なものを次の(1)~(3)の中から一つ選べ。$\fbox{ア}$
- 問2 3つの耐圧容器A、B、Cが、コックⅰとコックⅱのついた管でつながった装置がある。コックⅰとコックⅱを閉じたままで、容器Aの容積は5L、Bは2L、Cは3Lであり、容器同士をつなぐ管の容積は無視できるものとする。気体はすべて理想気体とみなし、27℃の水の蒸気圧は$3.6\times10^3$Pa、気体の水(液体)への溶解、液体の体積は無視できるものとする。
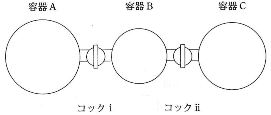
コックⅰとコックⅱを閉じたままで、容器Aにメタンを$9.0\times10^{-2}$mol、容器Bにアルゴンを$4.0\times10^{-2}$mol、容器Cに酸素を$9.0\times10^{-2}$mol封入した。
実験3:コックⅰを開いて、容器Aと容器B内の圧力が一定になるまで放置した。その間、装置全体の温度は27℃に保った。
実験4:実験3のあとコックⅱを開き、全体が一定の圧力になるまで放置した。その後、適切な方法で点火し、反応できる量のメタンを完全燃焼させた。冷却した後、装置全体を27℃に保った。
- [1] 実験3の際のアルゴンの分圧はいくらか。$\fbox{ク}$、$\fbox{ケ}$、$\fbox{サ}$に入る適切な数値をマークし、$\fbox{コ}$には符号を次の(1)と(2)の中から一つ選べ。
- $\fbox{ク}.\fbox{ケ}\times10^{\fbox{コ}\fbox{サ}}$ Pa
- 符号
- $\fbox{コ}$
- (1)-
- (2)+
- [2] 実験4の最後での全圧は何Paか。$\fbox{シ}$、$\fbox{ス}$、$\fbox{ソ}$に入る適切な数値をマークし、$\fbox{セ}$には符号を次の(1)と(2)の中から一つ選べ。
- $\fbox{シ}.\fbox{ス}\times10^{\fbox{セ}\fbox{ソ}}$ Pa
- 符号
- $\fbox{セ}$
- (1)-
- (2)+
- [1] 実験3の際のアルゴンの分圧はいくらか。$\fbox{ク}$、$\fbox{ケ}$、$\fbox{サ}$に入る適切な数値をマークし、$\fbox{コ}$には符号を次の(1)と(2)の中から一つ選べ。