日本大学化学2012年第6問
次の問1~問3に答えなさい。

- 問1 中性アミノ酸の水溶液を酸性にするとその構造式は、$\fbox{34}$となり、塩基性にすると、$\fbox{35}$の構造式となる。グルタミン酸は等電点が$\fbox{36}$側にあるので、中性付近では側鎖の$\fbox{37}$がイオン化し、分子全体として$\fbox{38}$イオンになる。
- 問2 アラニン、グルタミン酸、リジンの3種のアミノ酸が溶けている混合液を細いガラス管でろ紙に少量塗布した。そのろ紙をpH6.0の緩衝液で湿らせ、両端に直流電圧をかけて電気泳動した。それぞれのアミノ酸は下図のように分離した。アミノ酸(ア)、(イ)、(ウ)はそれぞれ$\fbox{39}$、$\fbox{40}$、$\fbox{41}$である。ただし、アミノ酸の泳動方向は、それぞれのアミノ酸が持つ電荷のみによって決まると考えてよい。
[$\fbox{34}$、$\fbox{35}$の解答群]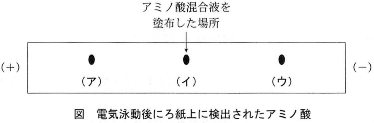
[$\fbox{36}$~$\fbox{41}$の解答群]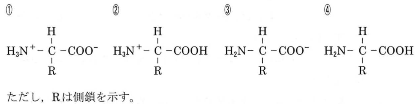
- (1) 陽
- (2) 塩基性
- (3) アラニン
- (4) グルタミン酸
- (5) リジン
- (6) 陰
- (7) 酸性
- (8) アミノ基
- (9) カルボキシ(ル)基
- 問3 ペプチドAはグルタミン酸、グリシン、システイン、セリン、フェニルアラニン、リジンをそれぞれ1つずつ含むアミノ酸6個からなるペプチドである。タンパク質を加水分解するトリプシンまたはキモトリプシンを用いてこのペプチドAを分解し、生成するペプチドを精製してその性質を調べたところ、下に示した[結果1]~[結果6]が得られた。ただし、トリプシンはこのペプチドA中のペプチド結合をリジンのカルボキシ(ル)基側で加水分解し、キモトリプシンはペプチド結合をフェニルアラニンのカルボキシ(ル)基側で加水分解する。
あるペプチドを例にして トリプシンがペプチド結合を加水分解する位置を下に示す。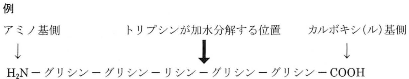
- [結果1] ペプチドAをトリプシンで加水分解するとペプチドⅠとペプチドⅡが得られた。
- [結果2] ペプチドⅠはキサントプロテイン反応が陽性であった。ペプチドⅠを酸により加水分解してアミノ酸とし、問2と同じ条件で電気泳動すると、陽極へ移動するアミノ酸とほとんど移動しないアミノ酸のみが検出された。
- [結果3] ペプチドⅡは硫黄反応が陽性で、アミノ基側のアミノ酸は光学異性体を持たないアミノ酸であった。ペプチドⅡを酸により加水分解してアミノ酸とし、問2と同じ条件で電気泳動すると、陰極へ移動するアミノ酸とほとんど移動しないアミノ酸のみが検出された。
- [結果4] ペプチドAをキモトリプシンで加水分解するとペプチドⅢとペプチドⅣが得られた。
- [結果5] ペプチドⅢはビウレット反応が陰性で、アミノ基側のアミノ酸はヒドロキシ(ル)基を持つアミノ酸であった。
- [結果6] ペプチドⅣはキサントプロテイン反応と硫黄反応がともに陽性であり、ペプチドⅣを酸により加水分解してアミノ酸とし、問2と同じ条件で電気泳動すると、陰極へ移動するアミノ酸とほとんど移動しないアミノ酸のみが検出された。
[$\fbox{42}$の解答群]
