聖マリアンナ医科大学物理2012年第4問
なめらかに動くピストンで仕切られているシリンダーがあり、ヘリウムが閉じ込められている。このシリンダーと、バルブを閉じた酸素ボンベを図2のように丈夫なパイプでつないだ。すべての機器と内部の気体の温度は気温と同じであり、シリンダー内の圧力は大気圧である。ヘリウムは大気と自由に熱のやりとりができるものとする。ヘリウムが単原子分子理想気体としてふるまうと仮定して、このボンベのバルブを開いたとき、図2のピストン右側で生じる現象について以下の各問に答えなさい。バルブの開閉でのボンベ内の温度・圧力変化は無視でき、圧力変化による変形や破損は機器のどこにも生じないものとする。気体定数$R=8.3$ 〔J/mol・K〕とする。
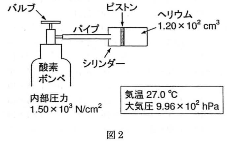 なお、$1\text{hPa}=100\text{Pa}$である。
なお、$1\text{hPa}=100\text{Pa}$である。

- 〔1〕 シリンダー内のヘリウムは何molかを数値で求めなさい。
- 〔2〕 バルブをきわめてゆっくりと開いて全開にした。このときシリンダー内のヘリウムは何という状態変化をしたかを気体の状態変化の名称で答えなさい。また、この状態変化でヘリウムの体積は何m3になったかを数値で求めなさい。
- 〔3〕 〔2〕を行った後で元の状態に組み直してから、バルブを一気に全開にした。このときのヘリウムの温度を知るために、理想気体の断熱変化で知られている関係式 \[ (圧力)\times(体積)^\gamma=一定 \] を利用したい。ここで \[ \gamma=1+\frac{R}{C_\text{V}} \\ R:気体定数 \\ C_\text{V}:定積モル比熱 \] である。単原子分子理想気体の$\gamma$を数値で求めなさい。
- 〔4〕 〔3〕のときのヘリウムの温度が何Kになるかを、ヘリウムの元の温度とバルブを開ける前後の圧力だけから知りたい。ヘリウムの温度に$T$ 〔K〕、圧力に$P$ 〔Pa〕の記号を用い、この記号にバルブ閉鎖時を0、バルブ全開時を1とした添字を使うこととして、バルブ全開時のヘリウムの温度$T_1$を求める式を〔3〕の式を利用して$T_0$、$P_0$、$P_1$、$\gamma$を用いて書きなさい。
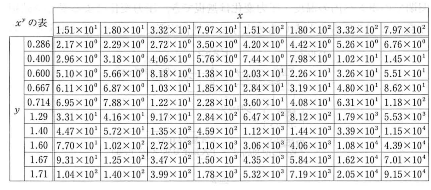
- 〔5〕 以下の表の適切な値を用い、〔4〕の$T_1$が何Kになるかを数値で求めなさい。
